Versuch zum Oxidationsvermögen einzelner Metalle
Materialen: Eisen-, Kupfer-, Silber- und Zinkblech; Eisen(II)sulfat-, Kupfer(II)sulfat-,Zink(II)sulfat, Silber(I)nitrat-Lösung.
Versuchsdurchführung:
Tauchen Sie blanke Streifen der Metalle Eisen, Kupfer, Silber und Zink nacheinander jeweils in die Sulfatl- und Nitratlösungen. Anschließen tragen Sie in die Tabelle ein, ob eine Reaktion stattfindet oder nicht.
Beobachtung:
Eisen(Ⅱ) sufat | Kupfer(Ⅱ) sulfat | Zink(Ⅱ) sulfat | Silber(I) nitrat | |
|---|---|---|---|---|
Eisen | ||||
Kupfer | ||||
Zink | ||||
Silber |
Auswertung:
1) Formulieren Sie ggf. die entsprechenden Redoxgleichung.
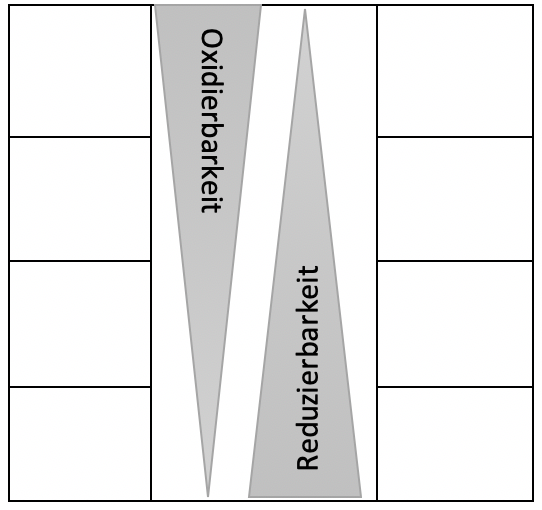
2) Sortieren Sie die Metalle nach ihrer Oxidierbarkeit und die Metallionen nach ihrer
Reduzierbarkeit in die Tabelle.
Eine Redoxreaktion ist eine chemische Reaktion, bei der ein Reaktionspartner Elektronen auf den anderen überträgt. Bei einer solchen Elektronenübertragungs-Reaktion finden also eine Elektronenabgabe (Oxidation) durch einen Stoff sowie eine Elektronenaufnahme (Reduktion) statt.
Bei der Oxidation steigt die Oxidationszahl.
Bei der Reduktion sinkt die Oxidationszahl.
https://www.tutory.de/entdecken/dokument/versuch-zum-oxidationsvermogen-einzelner-metalle-1


