Experiment: Flammenfärbung
Geräte
- Brenner
- Streichhölzer
- Tiegelzange
- Magensiastäbchen
- Tüpfelplatte
- Pinzette
Chemikalien
- LiCl
- NaCl
- CuCl2
- SrCl2
- nutzt die rauschende Brennerflamme
- das Magnesiastäbchen muss vor jedem Salz neu ausgeglüht werden
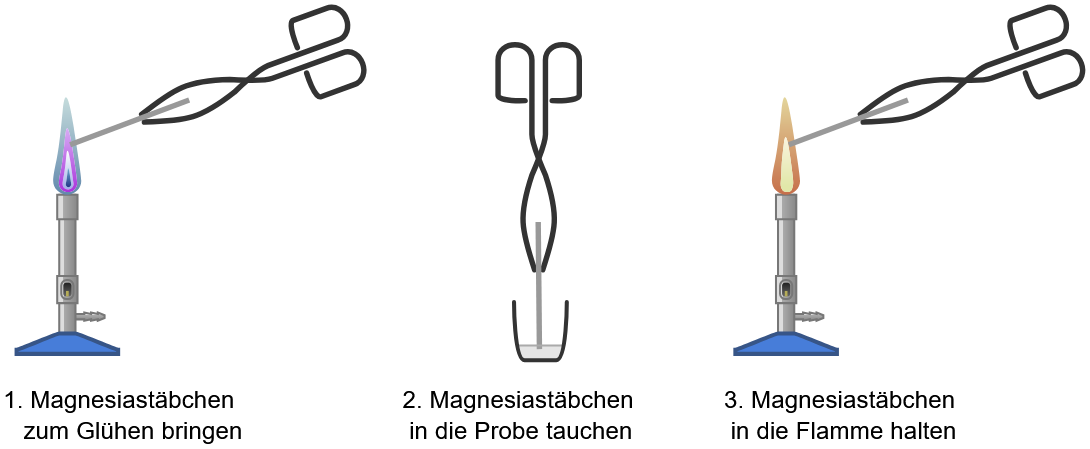
ACHTUNG! Das Magnesiastäbchen ist nach dem Glühen sehr heiß! Fasst es nur mit der Tiegelzange oder der Pinzette an!

Beobachtungstabelle
Auswertung
Salz
Flammenfarbe
1: LiCl
rot
2: NaCl
gelb
3: SrCl2
rot
4: CuCl2
grün
Kation
Anion
Salz-Name
Li+
Lithium-Ion
Cl-
Chlorid-Ion
Lithium-Chlorid
Na+
Natrium-Ion
Cl-
Chlorid-Ion
Natrium-Chlorid
Sr2+
Strontium-Ion
Cl-
Chlorid-Ion
Strontium-Chlorid
Cu2+
Cl-
Chlorid-Ion
Kupfer-Chlorid
https://www.tutory.de/entdecken/dokument/ab-flammenfaerbung
Die Ladung der Ionen hängt von ihrer Stellung im PSE ab - genauer gesagt von der in der das jeweilige Atom steht.
Lithium steht in der Hauptgruppe. Es gibt daher Elektron ab, um die stabile Edelgaskonfiguration zu erreichen. Damit besitzt das Ion Protonen und Elektronen. Es ist daher positiv geladen. Als Symbol schreibt man .
Strontium steht in der Hauptgruppe. Es gibt daher Elektronen ab, um die stabile Edelgaskonfiguration zu erreichen. Damit besitzt das Ion Protonen und Elektronen. Es ist daher positiv geladen. Als Symbol schreibt man .
Die Flammenfärbung wird genutzt, um unbekannte Stoffe zu untersuchen. Gib für die Bilder an, welche Ionen in den untersuchten Proben enthalten waren.



https://www.tutory.de/entdecken/dokument/ab-flammenfaerbung


