Um die Lizenzinformationen zu sehen, klicken Sie bitte den gewünschten Inhalt an.
Name:
Versuch zum Oxidationsvermögen einzelner Metalle
08.09.2019
Versuch zum Oxidationsvermögen einzelner Metalle
Beobachtung:
Eisen(Ⅱ) sufat | Kupfer(Ⅱ) sulfat | Zink(Ⅱ) sulfat | Silber(I) nitrat | |
|---|---|---|---|---|
Eisen | ||||
Kupfer | ||||
Zink | ||||
Silber |
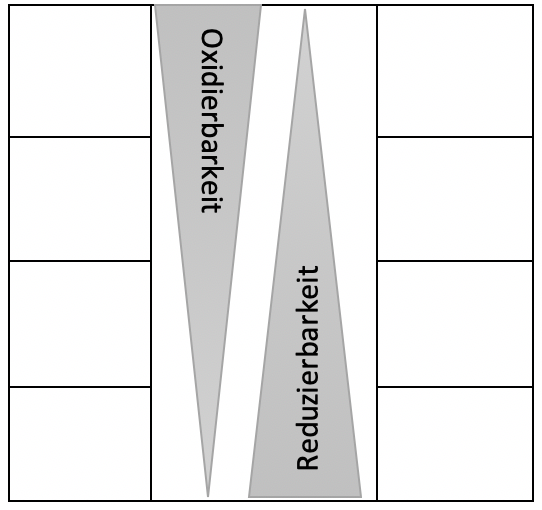
Redoxreaktion:
Eine Redoxreaktion ist eine chemische Reaktion, bei der ein Reaktionspartner Elektronen auf den anderen überträgt. Bei einer solchen Elektronenübertragungs-Reaktion finden also eine Elektronenabgabe (Oxidation) durch einen Stoff sowie eine Elektronenaufnahme (Reduktion) statt.
Bei der Oxidation steigt die Oxidationszahl.
Bei der Reduktion sinkt die Oxidationszahl.


