Mind-Map
Eine Mind-Map ist eine Visualisierungstechnik. Man verwendet dazu entweder ein weißes Blatt oder kann eine Mind Map auch digital erstellen.
In der Mitte steht das Thema der Mind Map. Dieses wird groß und deutlich hervorgehoben (Dicker schreiben, andere Farbe,...). Anschließend werden um dieses Thema Schlüsselbegriffe geschrieben, die mit Ästen mit dem Thema verbunden sind.
An diese Schlüsselbegriffe werden weitere Begriffe mithilfe von Ästen geschrieben. Man kann eine Mind Map daher beliebig oft vergrößern und erweiteren, je nachdem, was man schon über ein Thema weiß.
Beispiel:
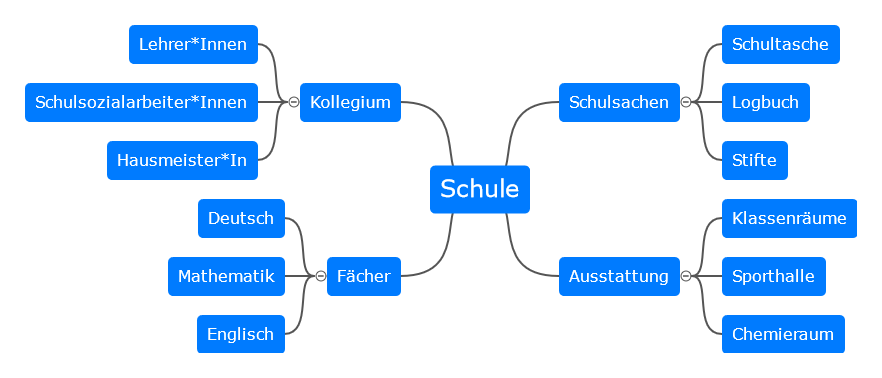
Nutze dazu die Informationen, die du bei den vorherigen Aufgaben bearbeitet hast.
Du kannst die Mind Map auf einem leeren Blatt Papier oder online gestalten
( https://kurzelinks.de/dhws).
https://www.tutory.de/entdecken/dokument/die-luft-und-ihre-bestandteile-8
Beantworte folgende Fragen schriftlich in deinem Heft. Schreibe die Frage mit ab.
- Was wollte Carl Scheele untersuchen?
- Welchen Zusammenhang gibt es, laut dem Chemiker Scheele, zwischen dem Feuer und der Luft?
- Wozu benötigt man beim Feuermachen einen Blasebalg?
- Was benötigt Feuer, damit es entstehen kann?
Kleiner Tipp: es sind drei Sachen, wobei nur eine im Text genannt wird. Die anderen entdeckst du auf dem Bild.
Die Luft hat so viele besondere Eigenschaften, dass sie demjenigen, der mit ihr Versuche anstellt, genug neue Entdeckungen bietet.
Auch das Feuer zeigt uns, dass es nicht ohne Luft erzeugt werden kann. Ich sah die Notwendigkeit ein, das Feuer zu kennen, weil ohne dies kein Versuch anzustellen ist.
Ich machte eine Menge von Versuchen, um diese Erscheinung genau zu ergründen.
Ich merkte aber bald, das man ohne Kenntnis der Luft kein wahres Urteil über das Feuer fällen könnte.
Textauszug von Carl Wilhelm Scheele (1742-1786)
https://www.tutory.de/entdecken/dokument/die-luft-und-ihre-bestandteile-8
Aussage
wahr
falsch
a)
Luft ist ein Gemisch aus Feststoffen.
b)
Luft besteht aus etwa 21 % Sauerstoff.
c)
Sauerstoff wird mit einem F abgekürzt.
d)
Pflanzen verbrauchen auch Sauerstoff.
e)
Der Hauptbestandteil der Luft ist Stickstoff mit knapp 80%.
f)
Menschen können mit dem Stickstoff wenig anfangen, dafür nutzen in Pflanzen.
g)
Argon ist das häufigste Edelgas, welches in der Luft vorkommt.
h)
Edelgase heißen Edelgase, weil sie edel sind, d.h. kaum bis gar nicht mit anderen Stoffen reagieren.
i)
Kohlenstoffdioxid ist für den Treibhauseffekt zuständig und nur zu etwa 0,04% in der Luft vorhanden.
j)
Feinstaub ist auch in der Luft, daher gibt es Umweltzonen in den Innenstädten.
https://www.tutory.de/entdecken/dokument/die-luft-und-ihre-bestandteile-8
Eigenschaften der Luftbestandteile
Sauerstoff ist ein chemisches Element mit dem Symbol O. Der so genannte elementare Sauerstoff besteht weitaus am häufigsten aus zweiatomigen Molekülen (O2). Sauerstoff ist ein farblosen und geruchloses Gas. Es lässt sich bei -183°C verflüssigen. Die bläuliche Flüssigkeit wird in blauen Stahlflaschen transportiert. Sauerstoff selbst brennt nicht, fördert aber die Verbrennung. Er reagiert leicht mit anderen Stoffen. Deshalb verläuft jede Verbrennung in reinem Sauerstoff heftiger als an der Luft. Sauerstoff wird mit der Glimmspanprobe nachgewiesen. Lebewesen verbrauchen Sauerstoff um ihre Körperfunktionen aufrecht zu erhalten und erzeugen dabei Kohlenstoffdioxid. Pflanzen wandeln das Kohlenstoffdioxid durch Photosynthese wieder in Sauerstoff um. Fische und andere Wasserlebewesen können unter Wasser atmen , weil sich Sauerstoff in Wasser löst. Bei 0°C lösen sich 49,1ml Sauerstoff in 1L Wasser. Wenn die Wassertemperatur ansteigt, nimmt die Löslichkeit ab.
Der Name Stickstoff bezeichnet das chemische Element aus dem Periodensystem der Elemente mit dem Symbol N. Molekularer Stickstoff ist mit 78 % der Hauptbestandteil der Luft. Lediglich eine kleine Anzahl von Mikroorganismen kann ihn nutzen, in ihre Körpersubstanz einbauen oder auch an Pflanzen abgeben. Pflanzen können den gasförmigen Stickstoff der Luft nicht unmittelbar nutzen. Stickstoff ist bei Raumtemperatur farb- und geruchlos, es ist nicht giftig oder brennbar. Stickstoff erstickt eine Flamme. Stickstoff reagiert kaum mit anderen Stoffen. Er wird deshalb auch als Schutzgas zum Verpacken von Lebensmitteln eingesetzt.
Kohlenstoffdioxid - oft auch als auch Kohlendioxid (CO2) bezeichnet - ist eine chemische Verbindung aus Kohlenstoff und Sauerstoff und spielt eine sehr wichtige Rolle bei der Photosynthese. Es ist ein farbloses und geruchloses Gas, dass sich gut in Wasser löst. Kohlenstoffdioxid erstickt die Flamme einer Kerze. Darum setzt man das Gas auch zum Feuerlöschen ein. Leitet man Kohlenstoffdioxid in Kalkwasser, wird dieses trübe. Die Trübung von Kalkwasser ist ein Nachweis für das Gas Kohlenstoffdioxid.
Gas | Sauerstoff | Stickstoff | Kohlenstoffdioxid |
|---|---|---|---|
chemsiche Abkürzung | |||
Farbe/ Geruch | |||
Anteil in der Luft | |||
Eigenschaften | |||
Nachweisreaktion |
Was passiert dort? Beschreibe.
- https://kurzelinks.de/Glimmspanprobe
- https://kurzelinks.de/Kalkwasser
- https://kurzelinks.de/reinerSauerstoff
https://www.tutory.de/entdecken/dokument/die-luft-und-ihre-bestandteile-8
Markiere unbekannte Begriffe oder schreibe sie heraus.
Schau dir auch die Bilder am Rand an. Sie helfen dir, den Text besser zu verstehen.
Bearbeite anschließend die Fragen auf den Seiten in deinem Heft.
https://www.tutory.de/entdecken/dokument/die-luft-und-ihre-bestandteile-8
https://www.tutory.de/entdecken/dokument/die-luft-und-ihre-bestandteile-8


