Um die Lizenzinformationen zu sehen, klicken Sie bitte den gewünschten Inhalt an.
Name:
Eigenschaften kristalliner Stoffe
05.12.2021
Versuch: Eigenschaften kristalliner Stoffe
Versuch 1a
Ihr benötigt:
- 3x Becherglas (Größe: ca. 100 mL)
- 1x Spatel
- 1x Leitfähigkeitsmessgerät
- Kochsalz (Natriumchlorid)
- Kaliumchlorid
- Zucker
Ihr benötigt:
- 3x Becherglas (Größe: ca. 100 mL)
- 1x Spatel
- 1x Leitfähigkeitsmessgerät
- Kochsalz (Natriumchlorid)
- Kaliumchlorid
- Zucker
- Untersucht alle Stoffe auf Aussehen und Geruch
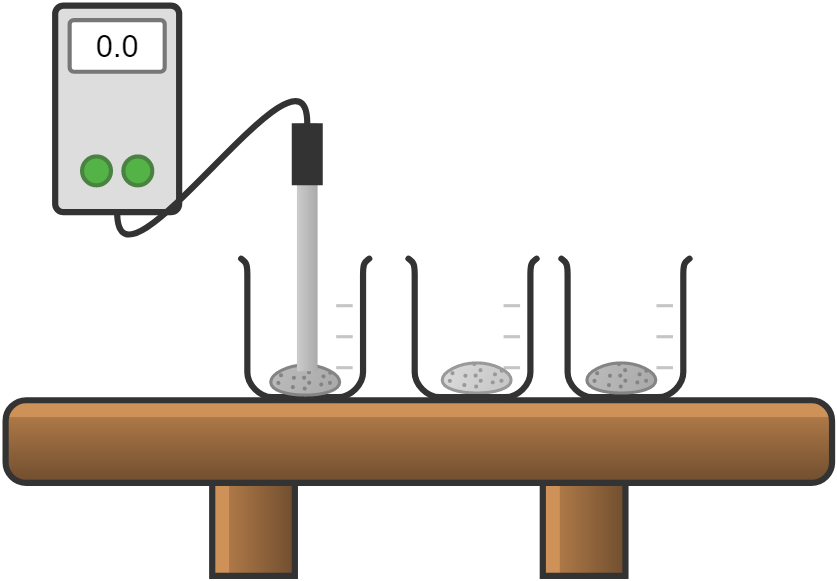
- Überprüft die elektrische Leitfähigkeit von Zucker, Kochsalz (Natriumchlorid) und Kaliumchlorid im festen Aggregatzustand. Gebt dazu jeweils zwei Spatelspitzen von jedem der drei Stoffe in drei verschiedene Bechergläser. Messt anschließend die Leitfähigkeit der Stoffe mit dem Leitfähigkeitsmessgerät.
- Notiert eure Beobachtungen und Messergebnisse in der Tabelle auf der Rückseite.
- Beschriftet den Versuchsaufbau.
Sicherheitshinweis!
Bei diesen Versuchen benötigt ihr eine Schutzbrille.
Versuch 1b
Für diesen Versuch benötigt ihr zusätzlich:
- 1x Becherglas (Größe: ca. 100 mL)
- pH-Papier
- destilliertes Wasser (Spritzflasche)
Für diesen Versuch benötigt ihr zusätzlich:
- 1x Becherglas (Größe: ca. 100 mL)
- pH-Papier
- destilliertes Wasser (Spritzflasche)
- Gebt etwas destilliertes Wasser in das leere Becherglas. Überprüft die elektrische Leitfähigkeit von destilliertem Wasser.
- Gebt ca. 50 mL destilliertes Wasser in das Becherglas mit dem Zucker, sodass der Zucker sich im Wasser lösen kann. Überprüft die elektrische Leitfähigkeit der Lösung.
- Gebt ca. 50 mL destilliertes Wasser in das Becherglas mit dem Kochsalz (Natriumchlorid), sodass das Kochsalz sich im Wasser lösen kann. Überprüft die elektrische Leitfähigkeit der Lösung.
- Gebt ca. 50 mL destilliertes Wasser in das Becherglas mit dem Kaliumchlorid, sodass es sich im Wasser lösen kann. Überprüft die elektrische Leitfähigkeit der Lösung.
- Bestimmt den pH-Wert aller Lösungen
- Notiert eure Beobachtungen in der Tabelle auf der Rückseite
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/eigenschaften-kristalliner-stoffe
https://www.tutory.de/entdecken/dokument/eigenschaften-kristalliner-stoffe
Name:
Eigenschaften kristalliner Stoffe
05.12.2021
Beobachtungen
Stoff
Aussehen,
Geruch
Löslichkeit
pH-Wert
elektr. Leitfähigkeit
Zucker (Feststoff)
-------
Kochsalz (Feststoff)
-------
Kaliumchlorid (Feststoff)
-------
destilliertes Wasser
-------
-------
Zucker-Lösung
Kochsalz-Lösung
Kaliumchlorid-Lösung
Auswertung
- Teile die untersuchten Feststoffe und Lösungen in elektrisch leitfähige und nicht elektrisch Leitfähige Stoffe bzw. Lösungen ein.
- Stelle eine Vermutung zur Erklärung der unterschiedlichen Leitfähigkeit der Salzlösungen und der Zuckerlösung auf.
- Stelle eine Vermutung zur Erklärung der unterschiedlichen Leitfähigkeit von festen und gelösten Salzen auf.
a)
b)
c)
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/eigenschaften-kristalliner-stoffe
https://www.tutory.de/entdecken/dokument/eigenschaften-kristalliner-stoffe


