Die Menge eines Stoffes kann man in der Chemie mit vier verschiedenen Maßangaben beschreiben. Alle sind gleichwertig zu verwenden, für manche Aufgaben braucht man aber eine bestimmte Maßangabe.
Die Umrechnung hängt meist von einem bestimmten, meist stoffspezifischen, Wert ab.
Die folgende Übersicht liefert dir alle notwendigen Informationen für die Umrechnung:
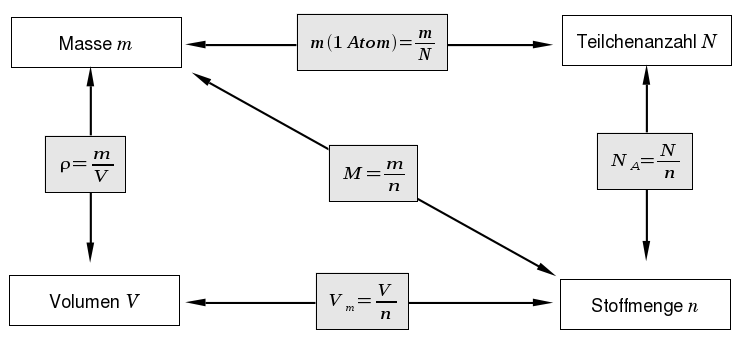
Informationen zu den Formelzeichen und deren Einheiten
Die Klammer um [g] bedeutet, das als Einheit für die Masse das Symbol g verwendet wird!
Die Dichte muss aus Tabellen abgelesen werden!
Die Molmasse lässt sich aus den Atommassen bestimmen, wobei M = m(1 Atom/Molekül) mit der Einheit [g/mol].
Das Molvolumen ist bei gasförmigen Stoffen 24,4l /mol (bei 25°C), bei festen und flüssigen Stoffen hat jeder Stoff einen anderen Wert!
Die Einheit [1/mol] bedeutet Stück pro Mol.
Informationen zur Konzentration
https://www.tutory.de/entdecken/dokument/f1148360


