Grundlagen der Chemie
Grundbegriffe:
Chemie ist die Lehre vom Aufbau der Materie.
Chemische Reaktionen ergeben neue Stoffe mit neuen Eigenschaften!
Vorgänge wie das Brechen von Holz oder das Schmelzen von Eis werden als physikalische Vorgänge bezeichnet (Die Stoffe verändern zwar ihre äußere Form oder ihren Aggregatzustand, ihre Substanz bleibt aber gleich).
Wird der Stoff aber in eine neue Substanz mit völlig neuen Eigenschaften umgewandelt, so handelt es sich um einen chemischen Vorgang (z. B. beim Verbrennen von Holz).
Wie ist die Materie aufgebaut?
Die meisten in der Natur vorkommenden Stoffe sind Gemenge (das heißt sie bestehen aus unterschiedlichen Bestandteilen).
Betrachtet man diese Gemenge unter dem Mikroskop, stellt man fest, dass einige von ihnen ein uneinheitliches Aussehen besitzen (z. B. Holz, Granit) – man nennt sie daher heterogene Gemenge.
Andere Gemenge dagegen besitzen ein einheitliches Aussehen (Kochsalzlösung, Luft) – man nennt sie daher homogene Gemenge.
Womit beschäftigt sich die Chemie?
Im Wesentlichen beschäftigt sich die Chemie mit drei Aufgabenbereichen:
▶ der Analyse von Stoffen (Woraus besteht der Stoff?).
▶ der Synthese von Stoffen (Wie kann man Elemente zusammenfügen und was geschieht dabei?).
▶ die Trennung von Gemengen in ihre Ausgangsstoffe.
https://www.tutory.de/entdecken/dokument/grundlagen-der-chemie-2
Warum werden Gemenge in ihre Ausgangsstoffe getrennt?
Manche Anwendungen erfordern extrem reine Substanzen. Zum Beispiel benötigt man zur Herstellung eines Computerchips sehr reines Silicium. Unter 109 Silicium-Atomen (1.000.000.000!!) darf sich maximal ein Fremdatom befinden.
Wir unterscheiden zwei Reinheitsgrade:
▶ technisch rein (ca. 95 Prozent rein)
▶ chemisch rein (über 99,5 Prozent rein)
Wie werden Gemenge in ihre Ausgangsstoffe getrennt?
In der Chemie gibt es unterschiedliche Verfahren zur Trennung von Gemengen. Dabei werden die physikalischen Eigenschaften der Bestandteile ausgenützt:
▶ Löslichkeit von Stoffen: Ermöglicht das Herauslösen von Stoffen aus einem Gemenge durch Extrahieren oder Filtrieren (z. B. die Zubereitung von Tee oder Kaffee).
▶ Dichte von Stoffen: Stoffe mit höherer Dichte setzen sich ab (z. B. sinkt Eisen im Hochofen ab, während das Gestein auf dem Eisen „schwimmt“).
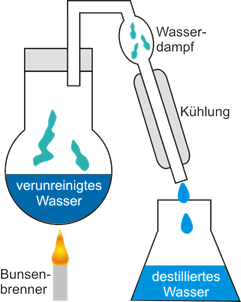
▶ Siedetemperatur von Stoffen: Stoffe verdampfen bei unterschiedlichen Temperaturen und können so voneinander getrennt werden (z. B. bei der Destillation von Rohöl, Wasser, Schnaps).
Ein weiteres Anwendungsbeispiel ist die Herstellung von destilliertem Wasser, das etwa benötigt wird, wenn kalkhaltiges Wasser ein Gerät auf Dauer kaputt machen würde (z. B. ein Bügeleisen) - siehe Abbildung auf der nächsten Seite.
https://www.tutory.de/entdecken/dokument/grundlagen-der-chemie-2
Begriffe, die du kennen solltest:
▶ Reinstoffe: Darunter versteht man Stoffe, die durch physikalische Verfahren nicht weiter aufgetrennt werden können, z. B. Wasser.
▶ Verbindungen: Verbindungen sind Reinstoffe, die sich durch chemische Reaktionen noch in weitere Stoffe zerlegen lassen. So kann z. B. Wasser in 2 Atome Wasserstoff und 1 Atom Sauerstoff zerlegt werden.
▶ Elemente: Darunter versteht man Reinstoffe, die sich nicht mehr in weitere Stoffe zerlegen lassen. So lassen sich z. B. der Wasserstoff und der Sauerstoff im Wasser nicht mehr in weitere Stoffe zerlegen.
https://www.tutory.de/entdecken/dokument/grundlagen-der-chemie-2
Und jetzt du:
heterogene Gemenge | homogene Gemenge | Reinstoffe | |
|---|---|---|---|
Kochsalz |
|
|
|
Beton |
|
|
|
Kristallzucker |
|
|
|
Gips |
|
|
|
Wein |
|
|
|
Rauch |
|
|
|
physikalischer Vorgang | chemischer Vorgang | |
|---|---|---|
eine Fensterscheibe beschlägt sich |
|
|
Milch wird sauer |
|
|
Eine Glühbirne wird eingeschaltet |
|
|
CO2 entweicht aus einer Gasflasche |
|
|
Ein Blatt färbt sich im Herbst rot |
|
|
Ein Ei wird hartgekocht |
|
|
https://www.tutory.de/entdecken/dokument/grundlagen-der-chemie-2


