- Die Fragen findet ihr auf der Rückseite.
- Die meisten Antworten findet ihr im Buch
Chemie 2
auf S. 174, 180-183 und 188 f.
https://www.tutory.de/entdecken/dokument/kreuzwortraetsel-chemie-saeure-base-neutralisation
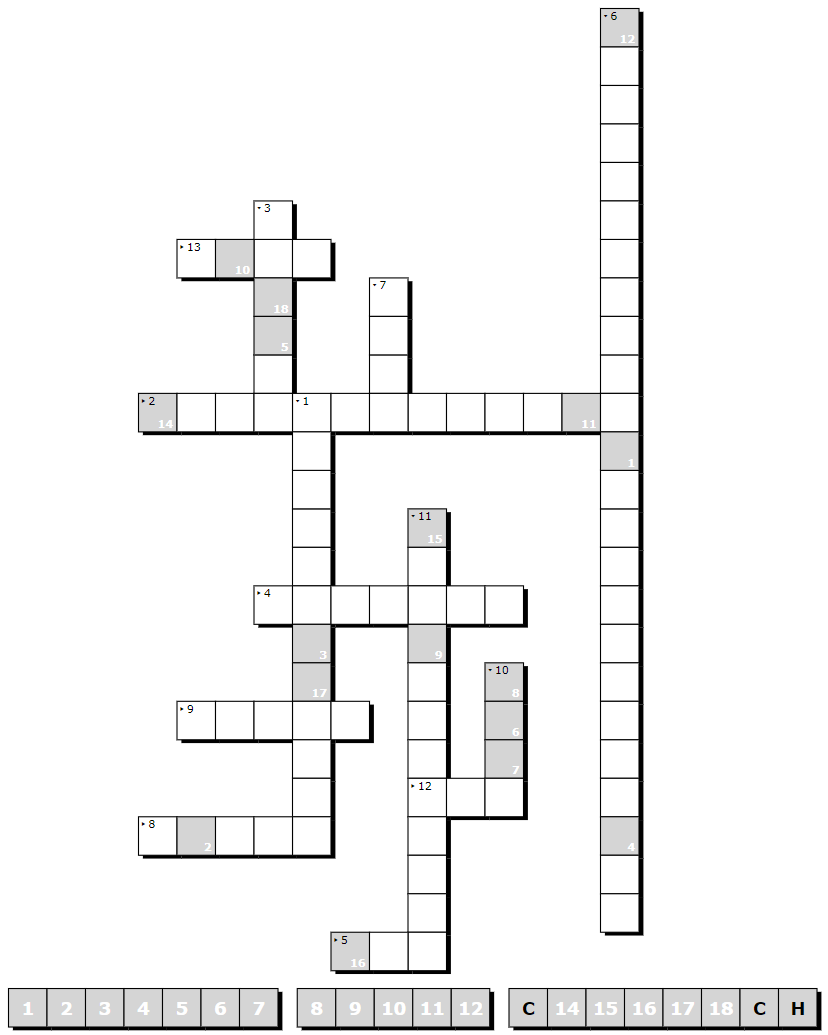
Fragen zum Kreuzworträtsel
1. Welche Teilchen sind in den wässrigen Lösungen aller Säuren enthalten?
2. Welche Teilchen sind in den wässrigen Lösungen aller Laugenenthalten?
3. Wenn ein Oxonium-Ion mit einem Hydroxid-Ion reagiert, wird ein Proton übertragen. Welcher Stoff entsteht dabei?
4. Statt Zwölf Eier
kann man auch Ein ... Eier
sagen. Um welches Wort geht es?
5. Sechs Komma null zwei zwei mal zehn hoch drei und zwanzig Teilchen nennen Chemikerinnen ein...
6. In einem bestimmten Volumen Wasser befindet sich eine bestimmte Stoffmenge Natriumchlorid. Wie heißt dieses Verhältnis von Stoffmenge zu Volumen in der Chemie?
7. Wie viel Mol Hydroxid-Ionen benötigt man, um zwei Mol Oxonium-Ionen zu neutralisieren?
8. Atome mit Ladung heißen...?
9. Wie heißen Moleküle, die ein elektrisch positives und ein elektrisch negativ geladenes Ende
besitzen?
10. Wie viele Elektronen befinden sich in der äußersten Schale von Neon?
11. Wie heißt die Regel, die besagt, dass Atome eine bestimmte Anzahl von Elektronen in der Valenzschale anstreben?
12. Welche Farbe nimmt Universalindikator in saurer Lösung an?
13. Welche Farbe nimmt Universalindikator in alkalischer (basischer) Lösung an?
Vertiefungsaufgaben
für Sprinter (und Pflicht für alle Weiterwähler)
Stoffmengenkonzentration c
Stoffmenge n
Volumen V
pH-Wert pH
Stoffmengenkonzentration c
Chemie 2. Bearbeite anschließend die folgenden Aufgaben:
- Berechne die Stoffmenge an Oxonium-Ionen in 2 L Salzsäure, wenn diese eine Stoffmengenkonzentration von c=5 mol/L besitzt.
- Berechne den pH-Wert von Essig mit einer Stoffmengenkonzentration von Oxonium-Ionen von c=0,025 mol/L.
- Um 1 L Salzsäure unbekannter Konzentration zu neutralisieren, wird Natronlauge (Konzentration: c=0,02 mol/L) hinzugegeben. Der Indikator zeigt die Neutralisation nach Zugabe von 0,2 L Natronlauge an. Berechne die Stoffmengenkonzentration der Salzsäure und ihren pH-Wert.
- Der Versuch wird mit Schwefelsäure (H2SO4) wiederholt. Dabei wird ebenfalls 1 L vorgelegt und die Konzentration der Schwefelsäure ist genauso groß wie die der Salzsäure. Bestimme, wie viel derselben Natronlauge in diesem Fall verbraucht wird.
https://www.tutory.de/entdecken/dokument/kreuzwortraetsel-chemie-saeure-base-neutralisation


