Um die Lizenzinformationen zu sehen, klicken Sie bitte den gewünschten Inhalt an.
Name:
Müdliche Nachprüfung in Chemie
02.08.2021
Mündliche Nachprüfung im Fach Chemie
1
In der Abbildung 1 siehst du zwei Teilgleichungen.
- Erkläre, was du bei den Teilgleichungen siehst und erläutere die Bedeutung aus chemischer Sicht.
- Um welche Bindungsart handelt es sich?
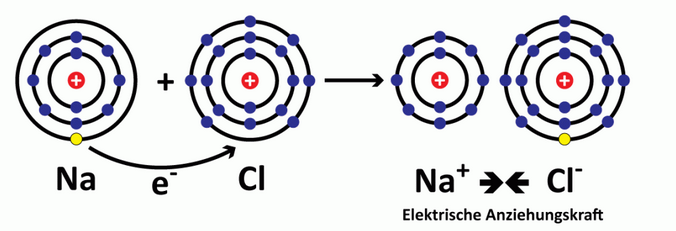
- Stelle die Reaktionsgleichung durch Zeichnen der Schalenmodelle von den beiden Atomen dar.
- Welche weiteren Bindungsarten kennst du in der Chemie? Nenne diese.
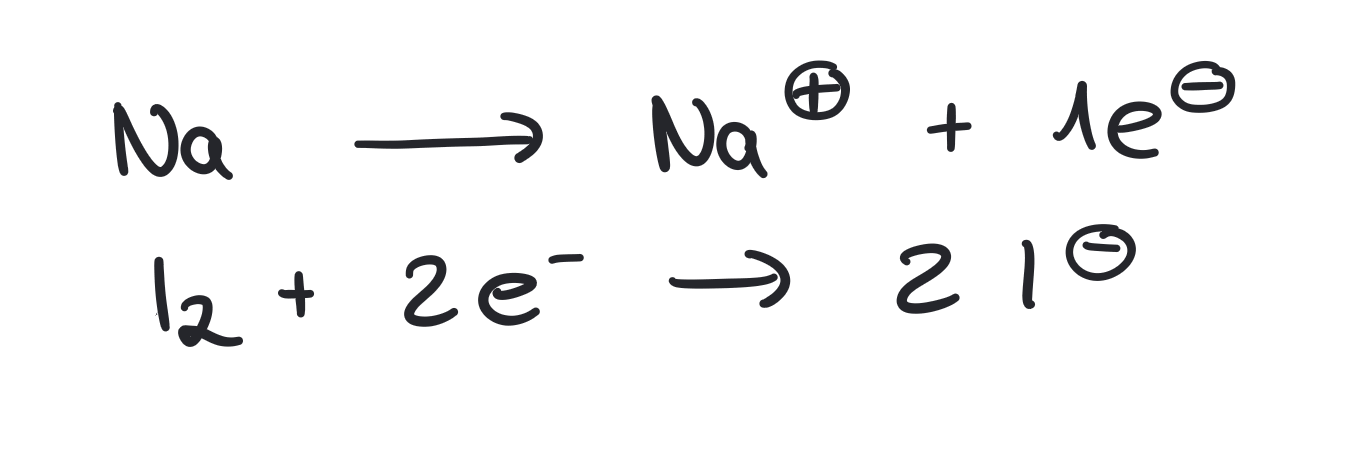
Abbildung 1
2
Die Abbildung 2 zeigt die Entstehung von Erdöl.
- Beschreibe in eigenen Worten die Entstehung .
- Wie und wo wird Erdöl gefördert?
- Nenne einen weiteren Namen, unter dem Erdöl bekannt ist.
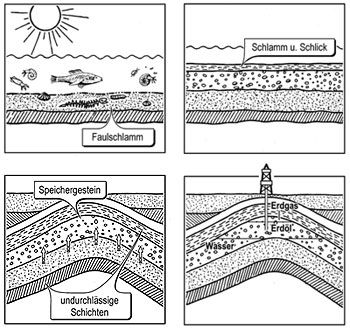
Abbildung 2: Erdölentstehung
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
Name:
Müdliche Nachprüfung in Chemie
02.08.2021
3
Die Nutzung des Erdöls in unserem Alltag ist nur möglich, wenn dieses weiter verarbeitet wird.
- Wo findet diese Weiterverarbeitung statt und wie nennt sich das Verfahren?
- Begründe, warum die Weiterverarbeitung auf diese Weise möglich ist
- Welche Produkte erhält man dabei? Nenne drei mögliche Produkte.
4
Die folgenden Aufgaben behandeln das Thema Alkane und Isomere.
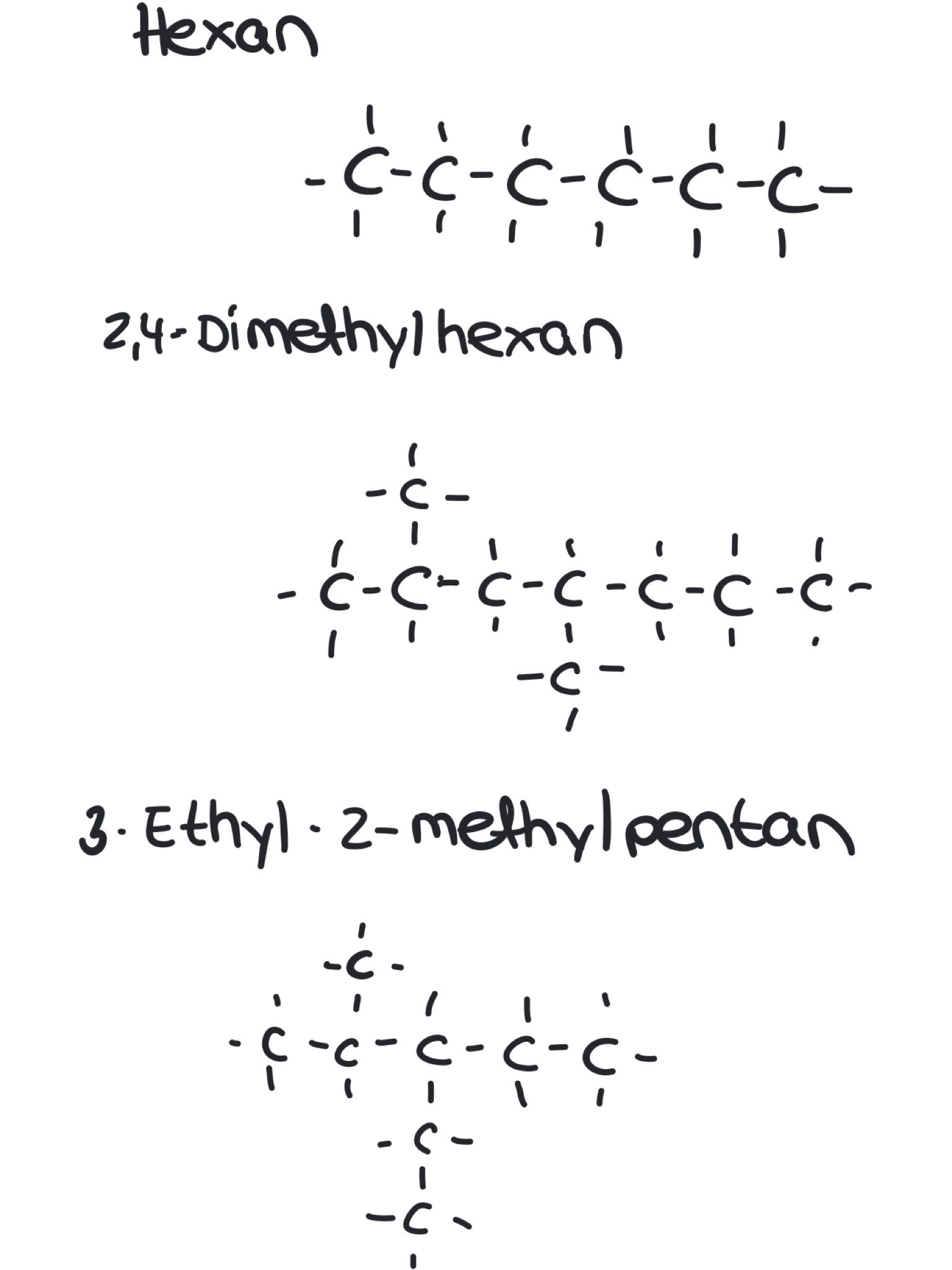
- Zeichne folgende Alkane und Isomere auf einem Blatt und erkläre, wie du dabei vorgegangen bist.
Hexan
2,4-Dimethylheptan
3-Ethyl2-methylpentan - Gib die Definition von Alkanen an und erkläre den Unterschied zwischen Alkanen und Isomeren.
- Die Abbildung 3 zeigt die Namen von Alkanen und Isomeren und die passenden Strukturformeln.
Ordne die Namen den Strukturformeln zu und begründe deine Wahl.
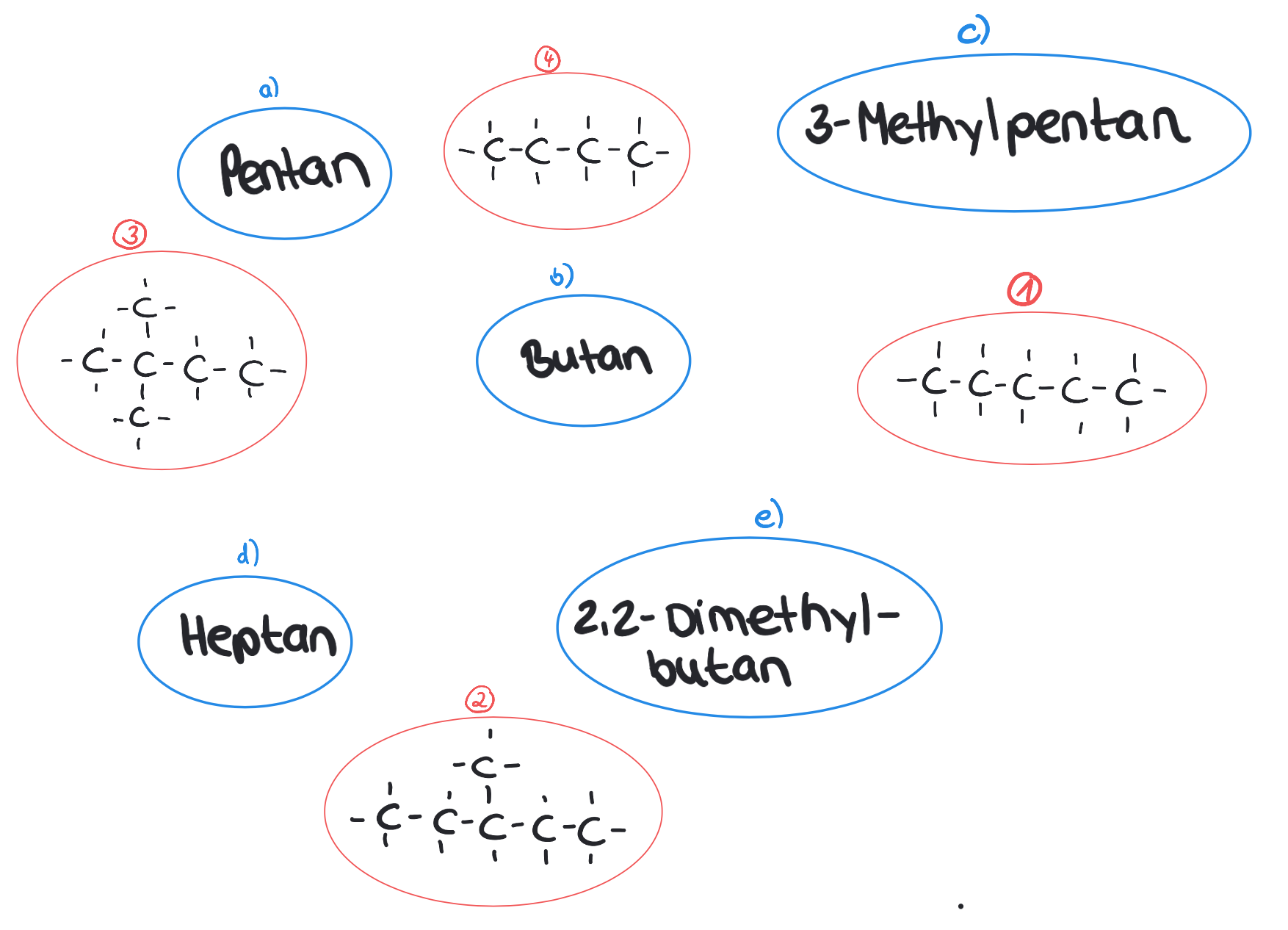
Abbildung 3
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
Name:
Müdliche Nachprüfung in Chemie
02.08.2021
Lösungen
1
In der Abbildung siehst du zwei Teilgleichungen.
- 1. Teilgleichung: ein Natriumatom gibt ein Elektron ab und wird zu einem positiv geladenen Natriumion (Kation).
2. Teilgleichung: Jedes Iod-Atom aus dem Iodmolekül nimmt ein Elektron auf und wird zu einem negativ geladenen Iod-Ion (Anion).
Bedeutung: Es handelt sich um eine Ionenbindung, dabei gibt ein Reaktionspartner die Elektronen ab und ein zweiter Reaktionspartner nimmt diese auf. Bei dieser Reaktion entsteht ein Salz. Natriumchlorid nennt man auch Kochsalz - Ionenbindung
- Elektronenpaarbindung (Atombindung)
2
Die Abbildung 2 zeigt die Entstehung vom Erdöl.
- Plankton sinkt nach dem Absterben auf den Meeresboden
Anaerobe Baktrien versetzten dieses unter Bildung von Faulschlamm
Überlagerung durch Ton- und Lehmschichten
Hoher Druck und Temperatur führen zur Umwandlung zu Erdöl
Erdöl gelangt durch die Poren nach oben bis zu einer undurchlässigen Gesteinsschicht,
dort reichert sich das Erdöl an - Durch Messung werden die Erdöllagerstätten gefunden, z.B. in der Nordsee. Dort wird eine Bohrinsel installiert und mit langen Bohrern das Erdöl nach oben gefödert. Der Abtransport erfolgt durch Tankschiffe.
- schwarzes Gold
3
Die Nutzung des Erdöls in unserem Alltag ist nur möglich, wenn dieses weiter verarbeitet wird.
- Raffinerie
Fraktionierte Destillation - Die Produkte im Rohöl haben eine unterschiedliche Siedetemperatur, weswegen sie durch Erhitzen getrennt werden können.
- Bitumen, Diesel, Benzin, Kerosin, schweres Heizöl
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
Name:
Müdliche Nachprüfung in Chemie
02.08.2021
4
Die folgenden Aufgaben behandeln das Thema Alkane und Isomere.
- Alkane sind lineare Kohlenwasserstoffverbindungen bestehend aus Einfachbindungen.
Formel: CnH2n+2
Unterschied: Alkane sind linear aufgebaut, Isomere haben die gleiche Summernformel wie die passenden Alkane, sind aber verzweigt. - a) = 1) lineare Kette aus fünf C-Atomen
b)=4) lineare Kette aus vier C-Atomen
c)=2) längste Kette besteht aus fünf C-Atomen, am 3. C-Atom ein Methylrest
d)= kein Partner
e)=3) längste Kette aus vier C-Atomen, am 2. C-Atom jeweils ein Methylrest
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
Name:
Müdliche Nachprüfung in Chemie
02.08.2021
Erwartungshorizont
Aufgabe
erfüllt
teilweise erfüllt
nicht erfüllt
1a)
1b)
1c)
1d)
2a)
2b)
2c)
3a)
3b)
3c)
4a)
4b)
4c)
Note
Unterschrift
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1
https://www.tutory.de/entdecken/dokument/mudliche-nachprufung-in-chemie-1


