Um die Lizenzinformationen zu sehen, klicken Sie bitte den gewünschten Inhalt an.
Name:
Reaktionsgschwindigkeit
18.03.2021
Kollisionstheorie
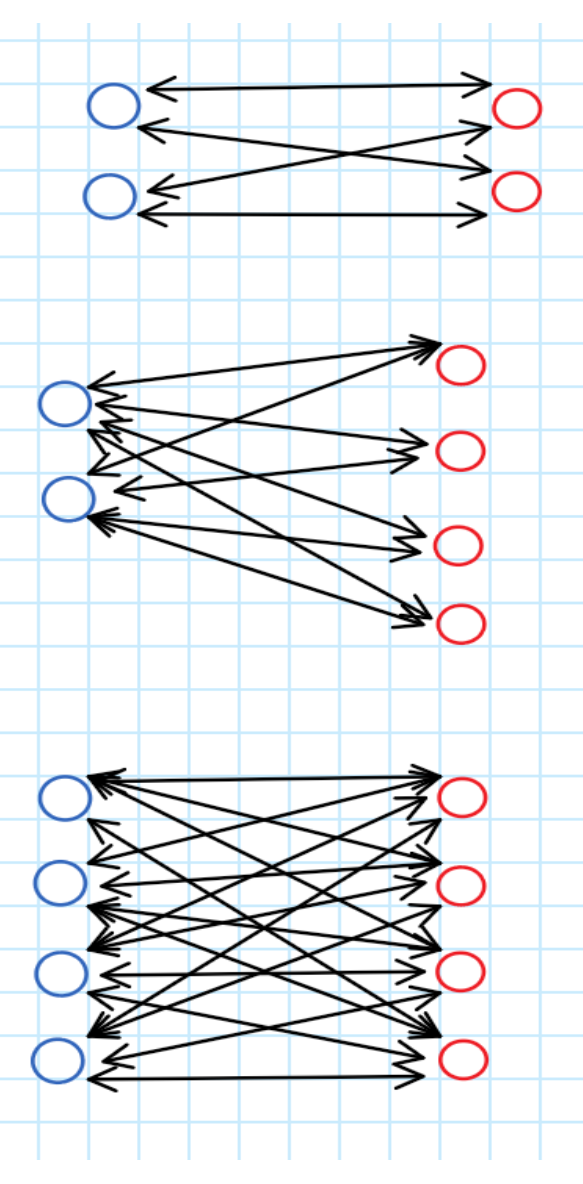
eigene Zeichnung
Zugrundeliegende Annahmen:
1
Durch Temperaturerhöhung bewegen sich die Teilchen schneller.
2
Nur wenn entsprechende Teilchen zusammentreffen, findet eine chemische Reaktion statt.
3
Je mehr Zusammenstöße, desto schneller läuft die Reaktion ab.
4
Um erfolgreiche reagieren zu können, benötigen die Teilchen eine Mindestenergie.
5
Beim Zusammenstoß müssen die Teilcen eine gewisse räumliche Orientierung zueinander haben, sonst findet keine Reaktion statt.
Vorgänge bei einer chemischen Reaktion(Verbrennung von Methan) - im Energiediagramm
Beispiel eines Energiediagramms
einer exothermen chemische Reaktion.
Aktivierungsenergie können Wärme,
eine angelegte Spannung oder LIcht sein.
einer exothermen chemische Reaktion.
Aktivierungsenergie können Wärme,
eine angelegte Spannung oder LIcht sein.
Angaben zu den Urhebern und Lizenzbedingungen der einzelnen Bestandteile dieses Dokuments finden Sie unter
https://www.tutory.de/entdecken/dokument/reaktionsgschwindigkeit
https://www.tutory.de/entdecken/dokument/reaktionsgschwindigkeit


