Chemische Reaktionen in unserem Körper
In unserem Körper laufen zahlreiche chemische Reaktionen ab. Ohne Chemie ist kein Leben denkbar!
Eine der wichtigsten chemischen Reaktionen in unserem Körper ist die Zellatmung. Sie findet in den Zellen statt. Es ist der Prozess, den Zellen verwenden, um Energie aus Nahrung zu gewinnen.
Dazu werden Sauerstoff und Glucose (ein Zucker) mit dem Blut zu den Zellen transportiert. Dort finden viele Reaktionen nacheinander statt, bei denen die Edukte schrittweise in Kohlenstoffdioxid (ein Gas) und Wasser umgewandelt werden. Dabei wird Energie frei. Zum Beispiel als Wärme. Ein Teil dieser Energie wird auf komplizierte Weise gespeichert. Sie kann später dort freigesetzt werden, wo sie im Körper benötigt wird.
Viele der biochemischen Reaktionen laufen von alleine nur sehr langsam ab oder starten nicht. Deshalb gibt es im Köper zahlreiche Enzyme, die die Reaktionen beschleunigen oder ermöglichen.
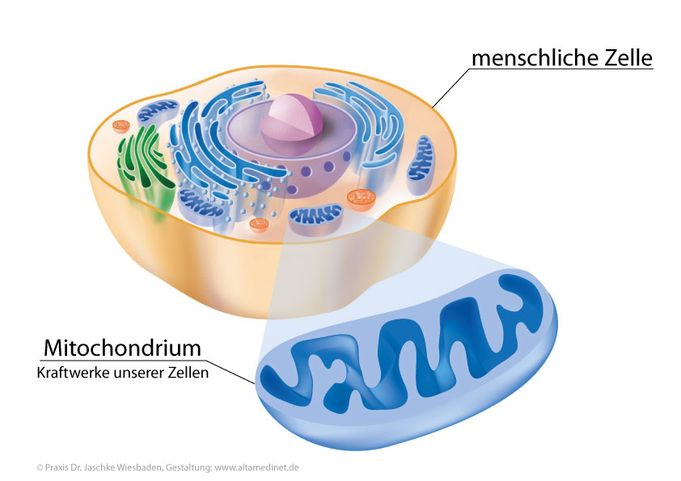
Erkläre diesen Begriff.
https://www.tutory.de/entdecken/dokument/uebungsaufgaben-chemische-reaktionen
Chemische Reaktionen in unserem Körper
In unserem Körper laufen zahlreiche chemische Reaktionen ab. Ohne Chemie ist kein Leben denkbar!
Eine der wichtigsten chemischen Reaktionen in unserem Körper ist die Zellatmung. Sie findet in den Zellen statt. Es ist der Prozess, den Zellen verwenden, um Energie aus Nahrung zu gewinnen.
Dazu werden Sauerstoff und Glucose (ein Zucker) mit dem Blut zu den Zellen transportiert. Dort finden viele Reaktionen nacheinander statt, bei denen die Edukte schrittweise in Kohlenstoffdioxid (ein Gas) und Wasser umgewandelt werden. Dabei wird Energie frei. Zum Beispiel als Wärme. Ein Teil dieser Energie wird auf komplizierte Weise gespeichert. Sie kann später dort freigesetzt werden, wo sie im Körper benötigt wird.
Viele der biochemischen Reaktionen laufen von alleine nur sehr langsam ab oder starten nicht. Deshalb gibt es im Köper zahlreiche Enzyme, die die Reaktionen beschleunigen oder ermöglichen.

Es findet ein Energieumsatz statt, weil ...
Es findet ein Stoffumsatz statt, weil ...
https://www.tutory.de/entdecken/dokument/uebungsaufgaben-chemische-reaktionen
Chemische Reaktionen in der Technik

Einer der wichtigsten chemischen Prozesse ist die Herstellung von Eisen. Eisen findet man in der Natur nicht in reiner Form, sondern nur als Verbindung. Zum Beispiel als Eisenoxid. Dieses muss aufbereitet werden. Dazu wird das Eisenoxid in riesigen Hochöfen auf 1800 °C erhitzt. In einem komplizierten Prozess entsteht dabei reines Eisen. Außerdem entweicht Sauerstoff als gasförmiges Nebenprodukt.

Für Autobatterien und große Akkumulatoren werden große Mengen an Schwefelsäure benötigt. Diese wird in großen Industrieanlagen hergestellt. Dazu wird das Gas Schwefel-Trioxid in Wasser eingeleitet. Es findet eine Reaktion statt, bei der Schwefelsäure entsteht. Der Prozess ist nicht ungefährlich, da sich das Reaktionsgemisch stark erhitzt.

Wasserstoff wird gerne als der Energieträger der Zukunft bezeichnet. Seine Herrstellung ist auch tatsächlich recht einfach. Dafür wird Wasser mit elektrischem Strom versetzt. Dabei zersetzt es sich in die zwei Gase Wasserstoff und Sauerstoff. Es muss allerdings sehr viel Strom aufgewendet werden, um das Wasser zu zerlegen ...
https://www.tutory.de/entdecken/dokument/uebungsaufgaben-chemische-reaktionen
Chemische Reaktionen in der Technik

Einer der wichtigsten chemischen Prozesse ist die Herstellung von Eisen. Eisen findet man in der Natur nicht in reiner Form, sondern nur als Verbindung. Zum Beispiel als Eisenoxid. Dieses muss aufbereitet werden. Dazu wird das Eisenoxid in riesigen Hochöfen auf 1800 °C erhitzt. In einem komplizierten Prozess entsteht dabei reines Eisen. Außerdem entweicht Sauerstoff als gasförmiges Nebenprodukt.

Für Autobatterien und große Akkumulatoren werden große Mengen an Schwefelsäure benötigt. Diese wird in großen Industrieanlagen hergestellt. Dazu wird das Gas Schwefel-Trioxid in Wasser eingeleitet. Es findet eine Reaktion statt, bei der Schwefelsäure entsteht. Der Prozess ist nicht ungefährlich, da sich das Reaktionsgemisch stark erhitzt.

Wasserstoff wird gerne als der Energieträger der Zukunft bezeichnet. Seine Herrstellung ist auch tatsächlich recht einfach. Dafür wird Wasser mit elektrischem Strom versetzt. Dabei zersetzt es sich in die zwei Gase Wasserstoff und Sauerstoff. Es muss allerdings sehr viel Strom aufgewendet werden, um das Wasser zu zerlegen ...
https://www.tutory.de/entdecken/dokument/uebungsaufgaben-chemische-reaktionen
Chemische Reaktion vs. Aggregatzustand
Bei einer chemischen Reaktion verändern sich die Eigenschaften von Stoffen. Manchmal denkt man daher, dass die Änderung des Aggregatzustandes ein Hinweis auf eine chemische Reaktion ist. Wir wollen uns angucken, warum das nicht immer stimmt!
- Beschreibe jeweils die Anordnung der Teilchen.
- Benenne die Aggregatzustände.
- Begründe, dass es sich nicht um eine chemische Reaktion handelt (Hinweis: Sind die Merkmale chemischer Reaktionen erfüllt?)
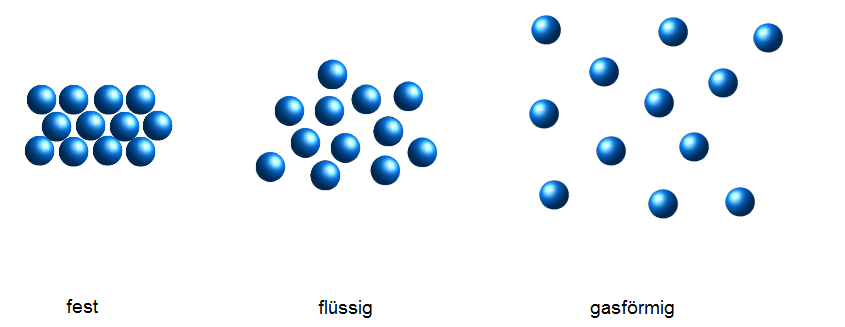
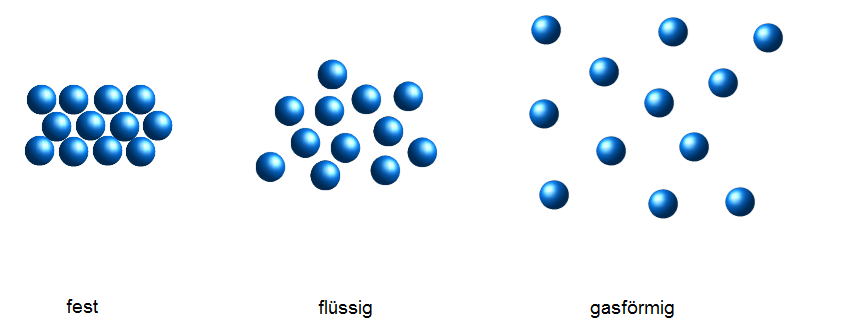
- Beschreibe jeweils die Anordnung der Teilchen.
- Benenne die Aggregatzustände.
- Begründe, dass es sich hier um eine chemische Reaktion handelt.
(Hinweis: 1. & 2. Merkmal)
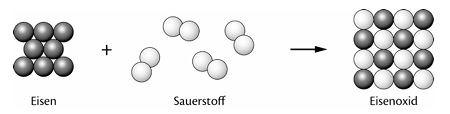
https://www.tutory.de/entdecken/dokument/uebungsaufgaben-chemische-reaktionen


